ANSM - Mis à jour le : 15/03/2021
REANUTRIFLEX OMEGA, émulsion pour perfusionAcides aminés, Glucose, Lipides Veuillez lire attentivement cette notice avant d’utiliser ce médicament car elle contient des informations importantes pour vous.1. Qu'est-ce que REANUTRIFLEX OMEGA, émulsion pour perfusion et dans quels cas est-il utilisé ?
2. Quelles sont les informations à connaître avant d'utiliser REANUTRIFLEX OMEGA, émulsion pour perfusion ?
3. Comment utiliser REANUTRIFLEX OMEGA, émulsion pour perfusion ?
4. Quels sont les effets indésirables éventuels ?
5. Comment conserver REANUTRIFLEX OMEGA, émulsion pour perfusion ?
6. Contenu de l’emballage et autres informations.
1. QU’EST-CE QUE REANUTRIFLEX OMEGA ET DANS QUELS CAS EST-IL UTILISE ?
Classe pharmacothérapeutique - code ATC : Solutions pour nutrition parentérale, associations -B05BA10
REANUTRIFLEX OMEGA contient des liquides et des substances appelées acides aminés et acides gras, qui sont essentiels pour permettre à l’organisme de se développer et de se rétablir. Le produit contient également des calories sous la forme de glucides et de lipides.
REANUTRIFLEX OMEGA est réservé à l’adulte.
REANUTRIFLEX OMEGA vous est administré lorsque vous êtes dans l’incapacité de vous alimenter normalement. Ce peut être le cas dans de nombreuses situations, par exemple lorsque vous récupérez d’une intervention chirurgicale, de blessures ou de brûlures ou lorsque vous ne pouvez pas absorber les aliments par l’intermédiaire de votre estomac et de vos intestins.
2. QUELLES SONT LES INFORMATIONS A CONNAITRE AVANT D’UTILISER REANUTRIFLEX OMEGA ?
N’utilisez jamais REANUTRIFLEX OMEGA :Par ailleurs, vous ne devez pas utiliser REANUTRIFLEX OMEGA si vous souffrez de l’un des troubles suivants :
·crise cardiaque ou accident vasculaire cérébral
·insuffisance rénale sévère en l’absence de traitement de substitution rénaleperturbations de la composition en sels de votre organisme
·insuffisance cardiaque sévère
oquantité excessive de lipides (graisses) dans le sang
oanomalies congénitales du métabolisme des acides aminés
otaux de sucre dans le sang anormalement élevé dont le contrôle nécessite l’administration de plus de 6 unités d’insuline par heure
oanomalies du métabolisme pouvant survenir après des opérations ou des blessures
ocoma d’origine indéterminée
oapport en oxygène insuffisant dans les tissus
otaux d’acide anormalement élevé dans le sang
Avertissements et précautionsAdressez-vous à votre médecin, à votre pharmacien ou à votre infirmier/ère avant d’utiliser REANUTRIFLEX OMEGA.
Veuillez informer votre médecin si :
·vous avez des problèmes au cœur, au foie ou aux reins ;
·vous souffrez de certains types de troubles métaboliques tels qu’un diabète, des taux anormaux de graisses dans le sang et des altérations de la composition en liquides et en sels ou de l’équilibre acido-basique de votre organisme.
Ce médicament est une solution sans électrolyte. Le personnel infirmier pourra également prendre les mesures nécessaires pour s’assurer que les besoins de votre corps en liquides et en électrolytes sont satisfaits. En plus de REANUTRIFLEX OMEGA, il est possible que l’on vous administre des nutriments (éléments nutritionnels) supplémentaires afin que vos besoins soient entièrement couverts.
EnfantsCe médicament ne doit pas être administré aux nouveau-nés, aux nourrissons et aux jeunes enfants âgés de moins de deux ans.
Autres médicaments et REANUTRIFLEX OMEGAInformez votre médecin, votre pharmacien ou votre infirmier/ère si vous prenez, avez récemment pris ou pourriez prendre tout autre médicament.
REANUTRIFLEX OMEGA peut interagir avec d’autres médicaments. Informez votre médecin, votre pharmacien ou votre infirmier/ère si vous prenez ou recevez l’un des médicaments suivants :
Sans objet.
Grossesse et allaitementSi vous êtes enceinte ou que vous allaitez, si vous pensez être enceinte ou planifiez une grossesse, demandez conseil à votre médecin ou pharmacien avant de prendre ce médicament. Si vous êtes enceinte, vous recevrez ce médicament uniquement si votre médecin ou pharmacien juge qu’il est absolument indispensable à votre rétablissement. Il n’existe pas de données disponibles sur l’utilisation de REANUTRIFLEX OMEGA chez la femme enceinte.
L’allaitement est déconseillé chez les mères recevant une nutrition parentérale.
Conduite de véhicules et utilisation de machinesCe médicament est normalement administré à des patients immobilisés, à l’hôpital ou dans une clinique par exemple, ce qui exclut la possibilité de conduire des véhicules ou d’utiliser des machines. Cependant, le médicament en lui-même n’a aucune influence sur l’aptitude à conduire des véhicules ou à utiliser des machines.
REANUTRIFLEX OMEGA contient du sodium.Ce médicament contient moins de 1 mmol (23 mg) de sodium par poche multicompartiments, c.-à-d. qu’il est essentiellement « sans sodium ».
3. COMMENT UTILISER REANUTRIFLEX OMEGA ?
Veillez à toujours utiliser ce médicament en suivant exactement les indications de votre médecin ou pharmacien. Vérifiez auprès de votre médecin ou pharmacien en cas de doute.
Ce médicament vous sera administré en perfusion intraveineuse (goutte à goutte), c’est-à-dire directement dans une veine à l’aide d’un petit tube. Ce médicament doit être administré uniquement dans une de vos grosses veines (centrales).
La durée maximale de perfusion d’une poche de nutrition parentérale est de 24h.
Votre médecin oupharmacien déterminera la quantité de ce médicament dont vous avez besoin et pendant combien de temps vous devrez être traité(e) par ce médicament.
Utilisation chez les enfantsLa sécurité et l’efficacité chez les enfants âgés de plus de 2 ans n’ont pas encore été établies. Aucune donnée n’est disponible.
Ce médicament ne doit pas être donné aux nouveau-nés, aux nourrissons et aux jeunes enfants âgés de moins de deux ans.
Si vous avez utilisé plus de REANUTRIFLEX OMEGA que vous n’auriez dû :Si vous avez reçu une quantité excessive de ce médicament, vous pourriez présenter ce que l’on appelle un « syndrome de surcharge » et les symptômes suivants :
·excès de liquides et troubles électrolytiques
·présence d’eau dans vos poumons (œdème pulmonaire)
·pertes d’acides aminés dans les urines et perturbation de l’équilibre en acides aminés
·vomissements, nausées
·frissons
·taux de sucre élevé dans le sang
·présence de glucose dans les urines
·déficit hydrique
·concentration du sang beaucoup plus importante que la normale (hyperosmolalité)
·altération ou perte de conscience due à un taux de sucre extrêmement élevé dans le sang
·augmentation du volume du foie (hépatomégalie) avec ou sans jaunisse (ictère)
·augmentation du volume de la rate (splénomégalie)
·dépôts de graisse dans les organes internes
·anomalies des paramètres de la fonction hépatique d’après les analyses de laboratoire
·diminution du nombre de globules rouges (anémie)
·diminution du nombre de globules blancs (leucopénie)
·diminution du nombre de plaquettes (thrombopénie)
·augmentation des globules rouges immatures (réticulocytose)
·destruction des cellules sanguines (hémolyse)
·hémorragie ou tendance aux saignements
·trouble de la coagulation du sang (mise en évidence par des modifications des temps de saignement, temps de coagulation, temps de prothrombine, etc...)
·fièvre
·taux de graisses élevés dans le sang
Si l’un de ces symptômes apparaît, la perfusion doit être immédiatement interrompue.
Si vous avez d’autres questions sur l’utilisation de ce médicament, demander plus d’informations à votre médecin, à votre pharmacien ou à votre infirmier/ère.
4. QUELS SONT LES EFFETS INDESIRABLES EVENTUELS ?
Les effets indésirables suivants peuvent être graves. Si l’un des effets indésirables suivants survient, prévenez immédiatement votre médecin ; il arrêtera de vous donner ce médicament :Rare (pouvant affecter jusqu’à 1 personne sur 1 000) :
·réactions allergiques, par exemple réactions cutanées, essoufflement, gonflement des lèvres, de la bouche et de la gorge, difficultés à respirer
Les autres effets indésirables comprennent :Peu fréquent (pouvant affecter jusqu’à 1 personne sur 100) :
Rare (pouvant affecter jusqu’à 1 personne sur 1 000) :
·coloration bleuâtre de la peau
·rougeur de la peau (érythème)
·élévation de la température corporelle
·diminution ou augmentation de la pression artérielle
Très rare (pouvant affecter jusqu’à 1 personne sur 10 000) :
·un excès de lipides peut entraîner un syndrome de surcharge graisseuse. Pour plus d’informations à ce sujet, veuillez-vous reporter au paragraphe « Si vous avez utilisé plus de REANUTRIFLEX OMEGA que vous n’auriez dû » dans la rubrique 3. Les symptômes disparaissent normalement après l’arrêt de la perfusion.
Fréquence indéterminée (ne peut être estimée sur la base des données disponibles) :
Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou, votre pharmacien ou à votre infirmier/ère. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Vous pouvez également déclarer les effets indésirables directement via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : www.signalement-sante.gouv.fr. En signalant les effets indésirables, vous contribuez à fournir davantage d’informations sur la sécurité du médicament.
5. COMMENT CONSERVER REANUTRIFLEX OMEGA ?
Tenir ce médicament hors de la vue et de la portée des enfants.
À conserver à une température ne dépassant pas +25 °C.
Ne pas congeler. En cas de congélation accidentelle, jeter la poche.
N’utilisez pas ce médicament après la date de péremption indiquée sur l’étiquette. La date de péremption fait référence au dernier jour de ce mois.
Conserver la poche dans l’emballage extérieur, à l'abri de la lumière.
Ne jetez aucun médicament au tout-à-l’égout ou avec les ordures ménagères. Demandez à votre pharmacien d’éliminer les médicaments que vous n’utilisez plus. Ces mesures contribueront à protéger l’environnement.
6. CONTENU DE L’EMBALLAGE ET AUTRES INFORMATIONS
Ce que contient REANUTRIFLEX OMEGA
|
Compartiment supérieur (solution de glucose) |
Dans 1 000 mL |
Poche de 625 mL |
Poche de 1 250 mL |
Poche de 1 875 mL |
|
Glucose monohydraté |
158,4 g |
99,00 g |
198,0 g |
297,0 g |
|
équivalent glucose |
144,0 g |
90,00 g |
180,0 g |
270,0 g |
|
Compartiment central (émulsion lipidique) |
Dans 1 000 mL |
Poche de 625 mL |
Poche de 1 250 mL |
Poche de 1 875 mL |
|
Triglycérides à chaîne moyenne |
20,00 g |
12,50 g |
25,00 g |
37,50 g |
|
Huile de soja raffinée |
16,00 g |
10,00 g |
20,00 g |
30,00 g |
|
Triglycérides d’acides gras oméga 3 |
4,000 g |
2,500 g |
5,000 g |
7,500 g |
|
Compartiment inférieur (solution d’acides aminés) |
Dans 1 000 mL |
Poche de 625 mL |
Poche de 1 250 mL |
Poche de 1 875 mL |
|
Isoleucine |
3,284 g |
2,053 g |
4,105 g |
6,158 g |
|
Leucine |
4,384 g |
2,740 g |
5,480 g |
8,220 g |
|
Lysine monohydratée équivalent lysine |
3,576 g |
2,235 g 1,990 g |
4,470 g 3,979 g |
6,705 g 5,969 g |
|
Méthionine |
2,736 g |
1,710 g |
3,420 g |
5,130 g |
|
Phénylalanine |
4,916 g |
3,073 g |
6,145 g |
9,218 g |
|
Thréonine |
2,540 g |
1,588 g |
3,175 g |
4,763 g |
|
Tryptophane |
0,800 g |
0,500 g |
1,000 g |
1,500 g |
|
Valine |
3,604 g |
2,253 g |
4,505 g |
6,758 g |
|
Arginine |
3,780 g |
2,363 g |
4,725 g |
7,088 g |
|
Histidine |
1,752 g |
1,095 g |
2,190 g |
3,285 g |
|
Alanine |
6,792 g |
4,245 g |
8,490 g |
12,73 g |
|
Acide aspartique |
2,100 g |
1,313 g |
2,625 g |
3,938 g |
|
Acide glutamique |
4,908 g |
3,068 g |
6,135 g |
9,203 g |
|
Glycine |
2,312 g |
1,445 g |
2,890 g |
4,335 g |
|
Proline |
4,760 g |
2,975 g |
5,950 g |
8,925 g |
|
Sérine |
4,200 g |
2,625 g |
5,250 g |
7,875 g |
|
Dans 1 000 mL |
Poche de 625 mL |
Poche de 1 250 mL |
Poche de 1 875 mL |
|
|
Teneur en acides aminés [g] |
56,0 |
35,0 |
70,1 |
105,1 |
|
Teneur en azote [g] |
8 |
5 |
10 |
15 |
|
Teneur en glucides [g] |
144 |
90 |
180 |
270 |
|
Teneur en lipides [g] |
40 |
25 |
50 |
75 |
|
Dans 1 000 mL |
Poche de 625 mL |
Poche de 1 250 mL |
Poche de |
|
|
Valeur énergétique sous forme de lipides (kJ [kcal]) |
1 590 (380) |
995 (240) |
1 990 (475) |
2 985 (715) |
|
Valeur énergétique sous forme de glucides (kJ [kcal]) |
2 415 (575) |
1 510 (360) |
3 015 (720) |
4 520 (1 080) |
|
Valeur énergétique sous forme de protéines (kJ [kcal]) |
940 (225) |
585 (140) |
1 170 (280) |
1 755 (420) |
|
Valeur énergétique non protéique (kJ [kcal]) |
4 005 (955) |
2 505 (600) |
5 005 (1 195) |
7 510 (1 795) |
|
Valeur énergétique totale (kJ [kcal]) |
4 945 (1 180) |
3 090 (740) |
6 175 (1 475) |
9 265 (2 215) |
|
Osmolalité [mOsm/kg] |
1 840 |
1 840 |
1 840 |
1 840 |
|
Osmolarité théorique [mOsm/L] |
1 330 |
1 330 |
1 330 |
1 330 |
|
pH |
5,0 – 6,0 |
5,0 – 6,0 |
5,0 – 6,0 |
5,0 – 6,0 |
acide citrique monohydraté (pour l’ajustement du pH), phospholipides d’œuf pour préparations injectables, glycérol, oléate de sodium, tout-rac-α-tocophérol, hydroxyde de sodium (pour l’ajustement du pH) et eau pour préparations injectables.
Qu’est-ce que REANUTRIFLEX OMEGA et contenu de l’emballage extérieur
Ce médicament prêt à l’emploi est une émulsion pour perfusion, c’est-à-dire qu’il est administré dans une veine à l’aide d’un petit tube.
REANUTRIFLEX OMEGA est fourni dans des poches souples multicompartiments contenant :
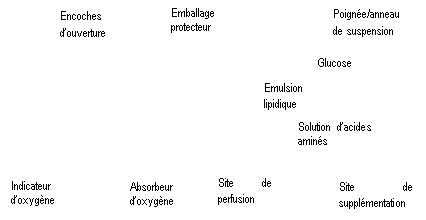
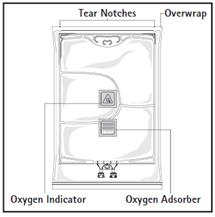
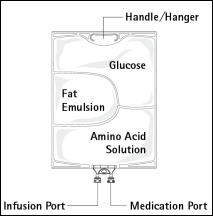
Figure A Figure B
Figure A : La poche multicompartiments est conditionnée dans un emballage protecteur. Un absorbeur d’oxygène et un indicateur d’oxygène sont placés entre la poche et l’emballage protecteur ; le sachet d’absorbeur d’oxygène est constitué d’une substance inerte et contient de l’hydroxyde de fer.
Figure B : Le compartiment supérieur contient une solution de glucose, le compartiment central contient une émulsion lipidique et le compartiment inférieur contient une solution d’acides aminés.
Les différents formats de conditionnement sont présentés dans des boîtes contenant cinq poches.
Présentations : 5 x 625 mL, 5 x 1 250 mL et 5 x 1 875 mL
Toutes les présentations peuvent ne pas être commercialisées.
Titulaire de l’autorisation de mise sur le marché
B. BRAUN MELSUNGEN AGCARL-BRAUN-STRASSE 1
34212 MELSUNGEN
ALLEMAGNE
Exploitant de l’autorisation de mise sur le marché
B. BRAUN MEDICAL26 RUE ARMENGAUD
92210 SAINT-CLOUD
B. BRAUN MELSUNGEN AGCARL-BRAUN-STRASSE 1
34212 MELSUNGEN
ALLEMAGNE
Noms du médicament dans les Etats membres de l'Espace Economique Européen
Ce médicament est autorisé dans les Etats membres de l'Espace Economique Européen sous les noms suivants :Conformément à la réglementation en vigueur.
La dernière date à laquelle cette notice a été révisée est :
[à compléter ultérieurement par le titulaire]
Des informations détaillées sur ce médicament sont disponibles sur le site Internet de l’ANSM (France).
Les informations suivantes sont destinées exclusivement aux professionnels de santé :Pas d’exigences particulières pour l’élimination.
Les médicaments de nutrition parentérale doivent être visuellement inspectés avant utilisation afin de vérifier l’absence de détérioration, de changement de coloration et d’instabilité de l’émulsion.
Ne pas utiliser les poches en cas de détérioration. L’emballage protecteur, le conditionnement primaire (poche) et les soudures non permanentes entre les compartiments doivent être intacts. Utiliser uniquement si les solutions d’acides aminés et de glucose sont limpides et incolores à jaune paille, et si l’émulsion lipidique forme un liquide homogène d’apparence blanc laiteux. Ne pas utiliser si les solutions contiennent des particules.
Après mélange des trois compartiments, ne pas utiliser si l’émulsion présente un changement de coloration ou des signes de séparation de phase (gouttes d’huile, film huileux). Cesser immédiatement la perfusion en cas de changement de coloration ou de signes de séparation de phase.
Avant d’ouvrir l’emballage protecteur, contrôler la couleur de l’indicateur d’oxygène (voir la figure A). Ne pas utiliser le produit si l’indicateur d’oxygène a viré au rose. Ne l’utiliser que si l’indicateur d’oxygène est jaune.
Préparation du mélange
Les règles d’asepsie doivent être strictement respectées lors de la manipulation du produit.
Pour ouvrir : Déchirer l’emballage protecteur en utilisant les encoches d’ouverture (fig. 1). Sortir la poche de son emballage protecteur. Jeter l’emballage protecteur, l’indicateur d’oxygène et l’absorbeur d’oxygène.
Inspecter visuellement le conditionnement primaire (poche) afin de vérifier l’absence de fuite. En cas de fuite, la poche doit être éliminée car sa stérilité ne peut être garantie.
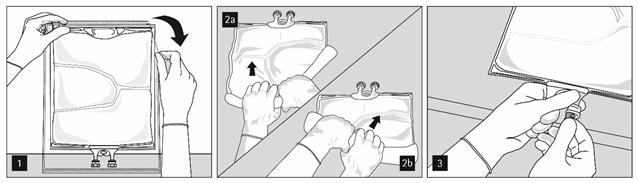
Pour ouvrir et mélanger successivement les compartiments, enrouler la poche avec les deux mains, en commençant par ouvrir la soudure pelable séparant le compartiment supérieur (glucose) du compartiment inférieur (acides aminés) (fig. 2a). Continuer ensuite à exercer une pression de façon à ouvrir la soudure pelable séparant le compartiment central (lipides) du compartiment inférieur (fig. 2b).
Ajout d’additifs
Après avoir retiré l’opercule en aluminium (fig. 3), il est possible d’ajouter des additifs compatibles via le site de supplémentation (fig. 4).
REANUTRIFLEX OMEGA peut être mélangé aux additifs suivants jusqu’aux limites supérieures des concentrations ou quantités maximales décrites ci-dessous après supplémentation. Les mélanges obtenus sont stables pendant 7 jours à une température comprise entre +2°C et +8°C ainsi que pendant 2 jours supplémentaires à +25°C.
Des informations sur les additifs décrits ci-dessus ainsi que la durée de conservation de ces additifs peuvent être fournies sur demande par le fabricant.
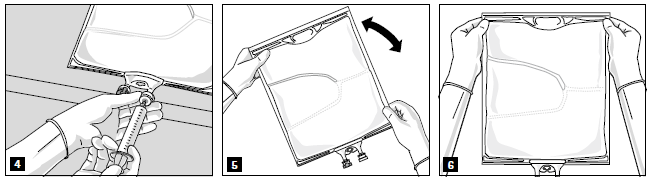 Mélanger soigneusement le contenu de la poche (fig. 5) et inspecter visuellement le mélange (fig. 6). L’émulsion ne doit présenter aucun signe de séparation de phase.
Mélanger soigneusement le contenu de la poche (fig. 5) et inspecter visuellement le mélange (fig. 6). L’émulsion ne doit présenter aucun signe de séparation de phase.
Le mélange est une émulsion d’huile dans l’eau d’apparence homogène et de couleur blanc laiteux.
Préparation de la perfusion
L’émulsion doit être systématiquement ramenée à température ambiante avant la perfusion.
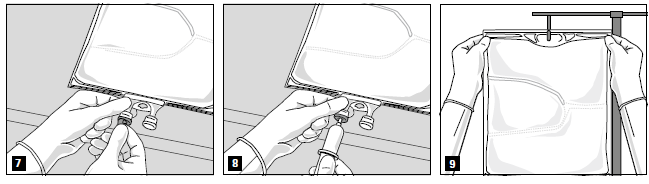
Retirer l’opercule en aluminium du site de perfusion (fig. 7) et fixer la ligne de perfusion (fig. 8). Utiliser une ligne de perfusion sans prise d’air ou fermer la prise d’air si une ligne de perfusion avec prise d’air est utilisée. Suspendre la poche sur une potence pour perfusion (fig. 9) et procéder à la perfusion selon la technique standard.
À usage unique strict. Le conditionnement et les résidus de produit inutilisés doivent être éliminés après utilisation.
Ne pas reconnecter des conditionnements partiellement utilisés.
Si des filtres sont utilisés, ils doivent être perméables aux lipides (taille des pores ≥ 1,2 µm).
Durée de conservation après retrait de l’emballage protecteur et après mélange des contenus de la poche
La stabilité physico-chimique après reconstitution du mélange de glucose, d’acides aminés et de lipides a été démontrée pendant 7 jours à une température comprise entre +2°C et +8°C ainsi que pendant 2 jours supplémentaires à +25°C.
Durée de conservation après ajout d’additifs compatibles
D’un point de vue microbiologique, le produit doit être utilisé immédiatement après ajout des additifs. S’il n’est pas utilisé immédiatement après l’ajout des additifs, les durées et conditions de conservation avant utilisation sont sous la responsabilité de l’utilisateur.
Après première ouverture (perforation du site de perfusion)
Le mélange doit être utilisé immédiatement après ouverture du conditionnement.
REANUTRIFLEX OMEGA ne doit pas être mélangé avec d’autres médicaments dont la compatibilité n’a pas été documentée.
REANUTRIFLEX OMEGA ne doit pas être administré en même temps que du sang dans la même ligne de perfusion en raison du risque de pseudo-agglutination.